Se trata del mavoglurant, probado en un estudio clínico riguroso. Si se amplían las pruebas y tienen éxito, podría convertirse en una herramienta clave en los tratamientos.

Durante décadas, el tratamiento del trastorno por uso de cocaína se sostuvo sobre un delicado andamiaje de terapias psicosociales, como la cognitivo-conductual, el acompañamiento terapéutico y el trabajo comunitario. Estrategias valiosas, sin duda, pero también insuficientes, especialmente en contextos atravesados por la exclusión, la recaída y el estigma. Frente a este panorama, la publicación de un nuevo estudio en la revista Science Translational Medicine abre un horizonte que hasta hace poco parecía inalcanzable: por primera vez, un fármaco mostró eficacia para reducir el consumo de cocaína en personas con adicción crónica.
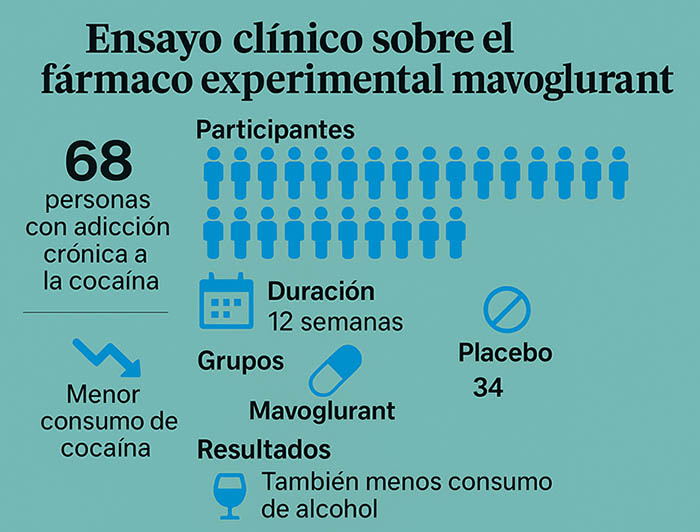
La Agencia de Noticias Científicas de la Universidad Nacional de Quilmes accedió al estudio completo, liderado por un grupo de investigadores originalmente vinculados a la farmacéutica Novartis. Se trata de un ensayo clínico aleatorizado, doble ciego y controlado con placebo —el estándar más riguroso para evaluar la eficacia de un medicamento— realizado durante 12 semanas en Estados Unidos. Participaron 68 adultos con diagnóstico de trastorno por uso de cocaína moderado a grave. La mitad recibió un tratamiento con mavoglurant, mientras que el resto fue asignado al grupo placebo.
Los resultados, medidos mediante análisis de orina y muestras de cabello, mostraron una reducción significativa en el consumo de cocaína y también en la ingesta de alcohol entre quienes recibieron el fármaco. Las diferencias se mantuvieron estables a lo largo de todo el período del estudio. El impacto clínico fue especialmente relevante entre los pacientes con patrones de consumo más intensos.
El mecanismo de acción de mavoglurant se basa en el bloqueo del receptor mGluR5, un componente clave del sistema de recompensa cerebral. Al inhibir este receptor, el fármaco interfiere con el circuito que impulsa el deseo compulsivo de consumir drogas. Aunque no elimina la adicción —una condición compleja y multifactorial—, puede brindar una ayuda farmacológica clave en el momento de mayor vulnerabilidad: cuando el impulso parece más fuerte que la voluntad.
Un nuevo mapa
Hasta ahora, los tratamientos disponibles para las adicciones a estimulantes como la cocaína, la metanfetamina o ciertos medicamentos recetados, se limitaban a estrategias no farmacológicas. En algunos casos, se exploraron fármacos “fuera de etiqueta” como el disulfiram o la naltrexona, pero los resultados fueron, en el mejor de los casos, dispares. La ausencia de una alternativa médica autorizada dejaba a millones de personas frente a un sistema de atención fragmentado, donde la contención psicológica y la intervención social se convertían en la única vía posible.
El ensayo con mavoglurant, aunque de escala aún reducida, marca un precedente que podría transformar ese escenario. La compañía suiza Stalicla SA, que obtuvo la licencia del fármaco en 2023, ya trabaja en nuevas fases clínicas con muestras más amplias y diversos perfiles poblacionales. La comunidad científica sigue el proceso con expectativa, pero también con cautela: ningún tratamiento aislado resolverá una problemática tan arraigada. Sin embargo, ofrecer una herramienta más —una pastilla que no promete milagros pero sí apoyo químico para resistir el impulso— puede ser decisivo en muchos casos.
En términos de salud pública, el avance no es menor. Según datos oficiales de Estados Unidos, más de 4,5 millones de personas cumplen con los criterios de trastorno por consumo de estimulantes. En Argentina, aunque las cifras son menores, la preocupación por el aumento del consumo de cocaína y sus efectos colaterales es compartida por profesionales de salud mental, médicos clínicos y equipos interdisciplinarios. La integración de un tratamiento farmacológico en estos dispositivos requerirá rediseñar políticas públicas, garantizar el acceso y, sobre todo, comprender que la adicción no es una elección, sino una enfermedad que merece una respuesta médica a la altura.
Hacia un modelo basado en evidencia
El estudio aún debe ser replicado en ensayos clínicos más amplios y diversos, que incluyan poblaciones de distintos perfiles demográficos, culturales y socioeconómicos. También es necesario investigar los posibles efectos adversos a largo plazo, la interacción con otros tratamientos y la eficacia en contextos reales fuera del entorno controlado del laboratorio clínico.
Mavoglurant no constituye, por el momento, una solución definitiva. Pero representa el inicio de una nueva etapa en la comprensión de las adicciones desde una perspectiva neurobiológica y médica. En combinación con intervenciones psicosociales, este enfoque mixto podría mejorar notablemente los índices de adherencia al tratamiento, reducir las tasas de recaída y ampliar el abanico de respuestas clínicas disponibles.
Con todo, el avance de la ciencia no suele ser rápido ni lineal. Pero cuando una investigación rigurosa logra modificar, aunque sea un poco, el rumbo de una problemática compleja, merece atención. Y en este caso, podría ser el primer paso hacia un nuevo paradigma terapéutico.