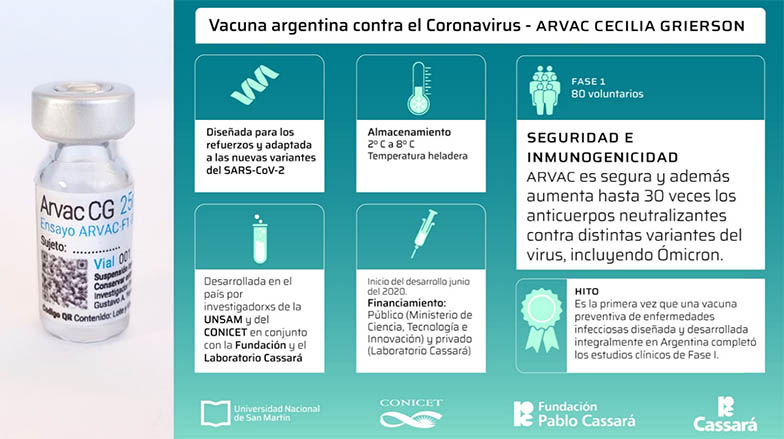
La “ARVAC Cecilia Grierson” completó la fase I de los ensayos clínicos y la Agencia I+D+i le otorgará 1.100 millones de pesos para realizar las fases II y III.
La ARVAC Cecilia Grierson recibirá un subsidio de 1.100 millones de pesos por parte de la Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación (Agencia I+D+i) parar llevar adelante los ensayos clínicos de las fases II y III de la vacuna desarrollada en conjunto por el CONICET, la Universidad Nacional de San Martín (UNSAM) y el Laboratorio Pablo Cassará. El apoyo económico obtuvo la aprobación del Ministerio de Ciencia, Tecnología e Innovación, del Ministerio de Economía y del propio presidente Alberto Fernández. Se espera que los estudios se realicen durante el primer trimestre de 2023 para que la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) pueda autorizar la vacuna durante el año próximo.
Fernando Peirano, presidente de la Agencia I+D+i, señaló: “Cuando las políticas públicas están presentes podemos desplegar todo nuestro potencial latente. Este es un gobierno que elige creer en el potencial de nuestras investigadoras e investigadores, que elige confiar en la capacidad argentina para desarrollar tecnologías innovadoras, que elige apoyar a la ciencia como camino hacia un desarrollo inclusivo y federal”.
Para los nuevos ensayos clínicos correspondientes a las fases II y III se desarrolló una nueva versión de la vacuna que incluye el antígeno en su variante Ómicron. De esta manera, permitirá evaluar una versión bivalente de la ARVAC que protegerá contra las sub-variantes BA.4 y BA.5.
Además, el estudio clínico se realizará en más de diez centros de investigación de todo el país. Esto aumentará la velocidad de implementación para obtener los resultados con mayor rapidez.
Fase I
En octubre se presentaron los resultados parciales de la fase I, etapa donde se evalúa la seguridad de la vacuna en una cantidad acotada de pacientes. El estudio se realizó con 80 personas sanas previamente vacunadas contra la Covid-19 y demostró ser segura y muy eficaz. Una dosis de refuerzo de ARVAC incrementa hasta 30 veces los anticuerpos neutralizantes contra las variantes del virus Ómicron, Gamma y Wuhan.
La fórmula ARVAC
Se basa en la tecnología de proteína recombinante, una fórmula segura y conocida que se utiliza desde hace décadas para fabricar la vacuna contra Hepatitis B que se da a niños recién nacidos, o contra HPV que se aplica a adolescentes. Está compuesta por un antígeno recombinante purificado (la región de la proteína spike que une al receptor ACE 2 llamado RBD versión gamma) con un adyuvante clásico como el gel de albúmina.
Esta vacuna se puede almacenar y transportar refrigerada (2-8 °C) y está diseñada para que en cuatro meses pueda actualizarse su principio activo para hacer frente a nuevas variantes del virus que escapen a la respuesta inmunológica de la población.